数据完整性缺陷案例
01
实验室数据完整性常见问题
02
FDA 483案例和警告信
03
未建立人员登录、授权、变更等程序
04
计算机化系统不符合要求
05
数据可靠性不符合要求
06
数据管理和文件记录
07
QC实验室管理不符合要求
3.高效液相色谱仪和红外光谱仪电脑时间未锁定,高效液相仪未进行计算机化系统验证,红外光谱仪电脑使用日志存在修改电脑时间现象。
本文内容转载于药械技术圈
热点文章
-
一文搞定制药设备清洁验证分析方法的开发与验证
2024-03-12
-
偏差流程要点分析和偏差处理成熟度的考量
2024-02-29
-
工艺验证“连续三批”的含义?
2024-02-29
-
【汇总】药品GMP现场检查常见问题
2024-02-13
-
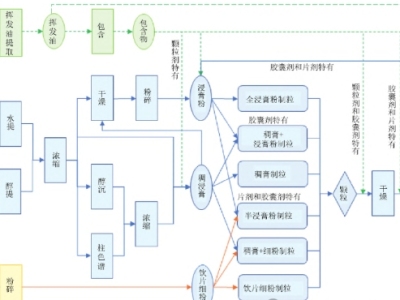
中药口服固体制剂制造分类系统: 工艺路线分类
2024-02-05
-
共线生产风险评估及清洁验证考虑要点
2024-02-04
-
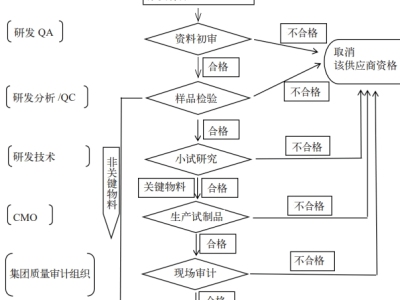
关于 B 证药品上市许可持有人供应商审计的思考
2024-03-01
-
新版附录1 对无菌灌装的影响
2023 年 8 月 25 日对于全球制药行业来说是非常重要的一天,新版 EU GMP 附录 1《无菌药品生产》(以下简称新版附录 1)于这一天正式生效。该文件对无菌灌装操作具有深远影响。对于新版附录 1 的生效,制药生产企业需要思考哪些问题?设备供应商(如星德科)又该如何帮助促进该文件的落实呢?
作者:Johannes Rauschnabel 博士
-
药厂立体库仓储方案仿真研究
-
洁净空调箱功能段的合理配置
-
基于微生物的控制对制药纯化水存储分配系统的优化设计
-
即将开幕,报名从速|2024PHT·固体制剂高质量发展论坛盛邀您的参与!
-
计算机系统在制药行业追溯体系应用中存在的问题与解决措施










评论
加载更多