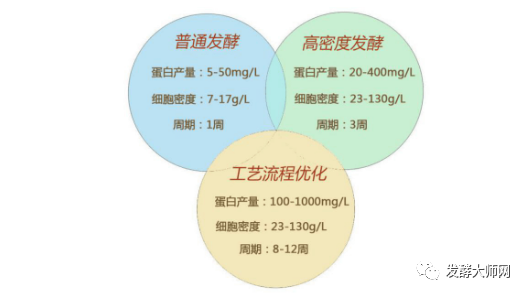
发酵工艺:蛋白类制品的大规模发酵制备及其一般纯化工艺
2.2 间接反馈控制
2.3 直接反馈控制
控制底物浓度—补料由发酵过程中碳源的浓度决定。(例如在发酵罐有实时的葡萄糖分析仪监测)大肠杆菌菌株高密度发酵研究,通过在600nm处测得细胞的OD值。
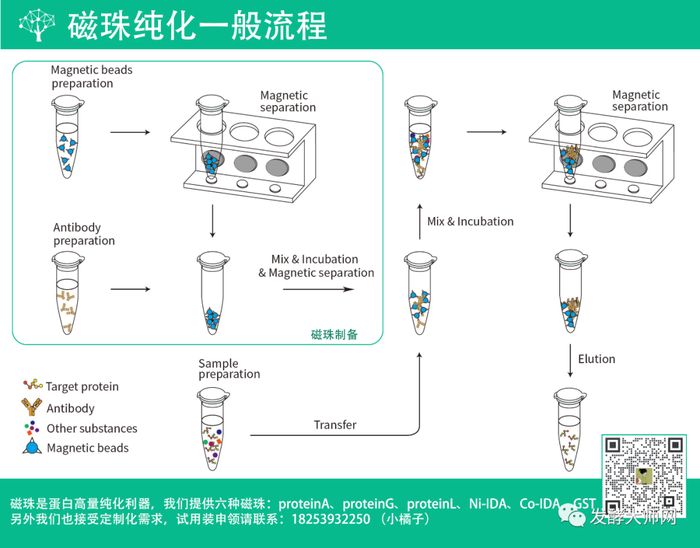
蛋白纯化策略侧重于在提高蛋白纯度的同时减少蛋白表达量的损失。因此我们常采用多种纯化方式混合纯化的方法,常用的纯化方法有以下四种:
3.1 亲和纯化
利用目的蛋白与其特异性配体之间的亲和力分离蛋白;固定化金属离子亲合层析(Immobilized metal ion affinity chromatography, IMAC),简称金属螯合亲合层析,是一种新型的应用于原核蛋白纯化的技术。该方法通过蛋白质表面的一些特殊的氨基酸,使之与金属离子发生相互作用,从而对蛋白质进行亲和纯化。这些作用包括配价键结合、静电吸附、共价键结合等,其中以6个组氨酸残基组合的融合标签(His-Tag)在原核蛋白表达中的应用最为显著。
3.2 离子交换色谱法
将离子交换剂与目的蛋白的电荷结合,通过改变PH或增加离子强度的缓冲液洗脱目的蛋白;离子交换色谱是蛋白纯化技术中常用的一种纯化方法,其原理是指被分离物质所带的电荷可与离子交换剂所带的相反电荷结合,这种带电分子与固定相之间的结合作用是可逆的,在改变pH或者用逐渐增加离子强度的缓冲液洗脱时,离子交换剂上结合的物质可与洗脱液中的离子发生交换而被洗脱到溶液中。由于不同物质的电荷不同,其与离子交换剂的结合能力也不同,所以被洗脱到溶液中的顺序也不同,从而被分离出来。
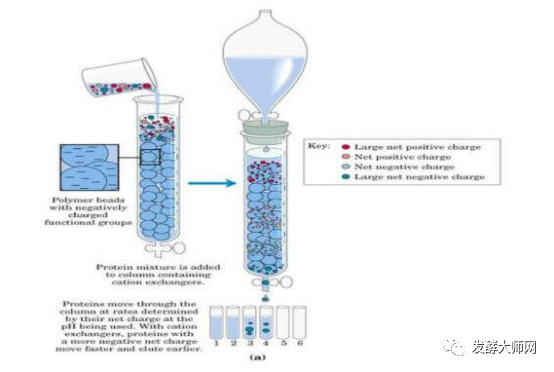
离子交换剂是由不溶于水的网状结构高分子聚合物骨架构成,骨架上有许多共价结合的带电基团,如果侧链是带正电基团,就可与带负离子相结合,称为阴离子交换剂,吸附带负电蛋白质。如果侧链是带负电的基团,则称为阳离子交换剂。强离子交换树脂在宽pH范围内保持离子化,而弱离子交换树脂只在窄pH值内离子化。
3.3 凝胶过滤色谱法
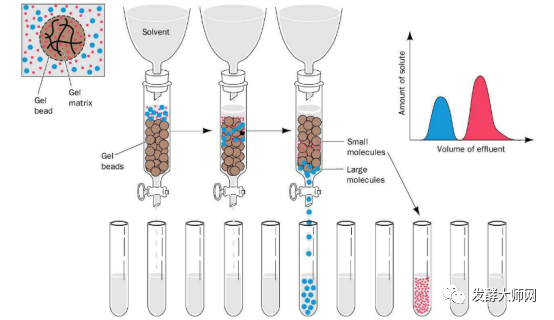
3.4 疏水色谱法
疏水色谱法是采用具有适度疏水性的填料,以含盐水溶液作流动相,借助于溶质与固定相间的疏水相互作用实现分离纯化的方法。
3.5 高效液相色谱法


此外高效液相色谱还有色谱柱可反复使用、样品不被破坏、易回收等优点;高效液相色谱的缺点是有“柱外效应”。在从进样到检测器之间,除了柱子以外的任何死空间(进样器、柱接头、连接管和检测池等)中,如果流动相的流型有变化,被分离物质的任何扩散和滞留都会显著地导致色谱峰的加宽,柱效率降低。
内容来源:发酵大师网
责任编辑:胡静 审核人:何发
热点文章
-
一文搞定制药设备清洁验证分析方法的开发与验证
2024-03-12
-
偏差流程要点分析和偏差处理成熟度的考量
2024-02-29
-
工艺验证“连续三批”的含义?
2024-02-29
-
【汇总】药品GMP现场检查常见问题
2024-02-13
-
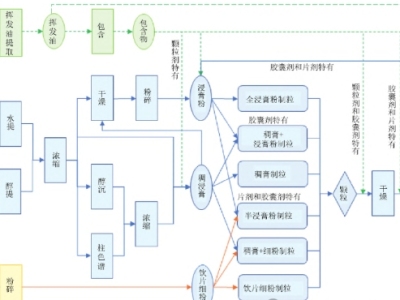
中药口服固体制剂制造分类系统: 工艺路线分类
2024-02-05
-
共线生产风险评估及清洁验证考虑要点
2024-02-04
-
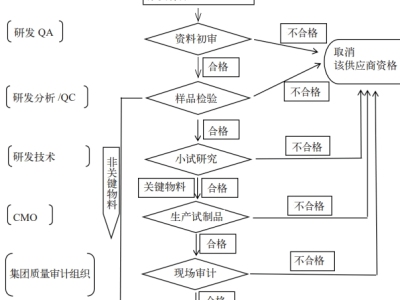
关于 B 证药品上市许可持有人供应商审计的思考
2024-03-01
-
紫外光谱检测自制熊果酸片剂的含量
本研究采用紫外分光光度法测定自制熊果酸片剂中熊果酸含量。以甲醇为溶剂,利用全波长对熊果酸溶液进行全波长扫描,并建立标准曲线。检测结果是熊果酸紫外最大吸收波长为 203.5 nm,回归方程为 y=0.0038x+0.1372,r=0.9987。加样回收率为 95.5%,RSD 为 1.43%。结果表明本方法操作简单、快速、灵敏,线性关系良好,可用于熊果酸片剂的质量控制。
作者:韩萌萌
-
一种提高醇沉沉渣排放速度的方法
-
收藏 | 统计方法在药品工艺验证中的应用
-
火焰原子吸收光谱法测定左氧氟沙星氯化钠注射液中氯化钠的含量
-
新版附录1 对无菌灌装的影响
-
药厂立体库仓储方案仿真研究









评论
加载更多