原料药或制剂稳定性研究那些事
Part
1
Part
2
Part
3

Part
4
Part
5
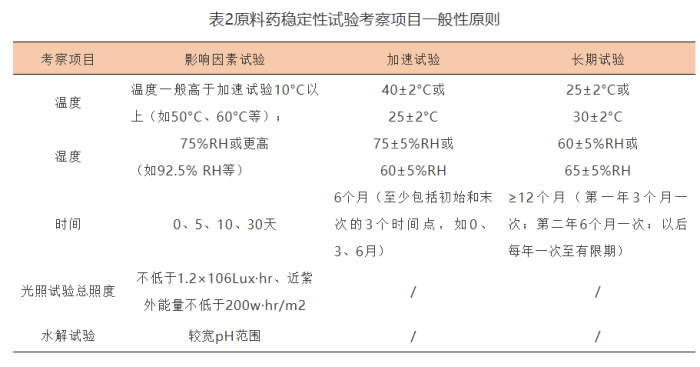
表3 制剂稳定性样品考察批次要求
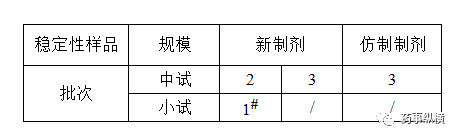

#:中间试验建议的考察时间为12个月,应包括所有的考察项目,检测至少包括初始和末次的4个时间点(如0、6、9、12月);如长期试验的放置条件为30±2°C/65%±5%RH,则无需进行中间条件试验。

#:长期试验是在25°C±2°C/40%RH±5%RH或是在30°C±2°C/35%RH±5%RH条件下进行,由研究者自行决定。
|
|
|
|
|
|
|
|
|
|
|
|

Part
6
Part
7
Part
8
表9 括号法设计示例

表10 某制剂两个规格关于时间点的矩阵设计示例“二分之一简化”
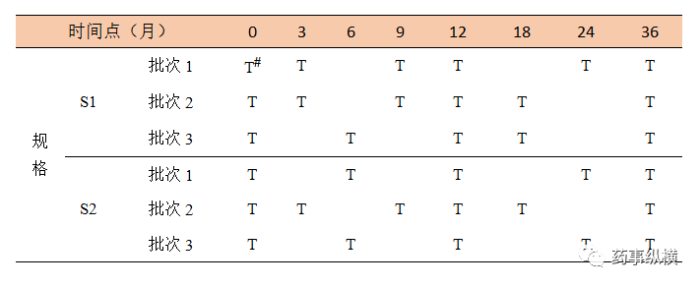
表11 某制剂两个规格关于时间点的矩阵设计示例“三分之一简化”
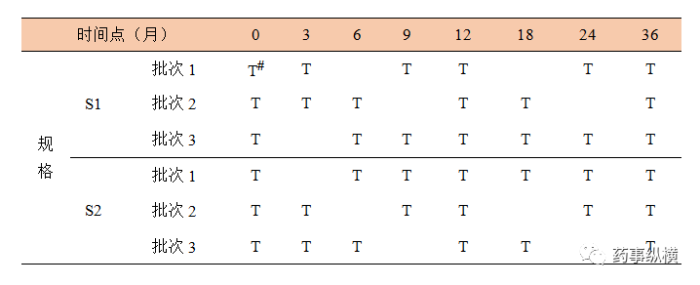
Part
9
参考文献
[1] CDE,化学药物(原料药和制剂)稳定性研究技术指导原则,2015年第3号
[2] FDA,Guidance for Industry ANDAs: Stability Testing of Drug Substances and Products,June 2013
[3] ICH Q1A(R2): Stability Testing of New Drug Substances and Products,Feb 2003
[4] CDE,化学药品新注册分类申报资料要求,2015年第80号
[5] CDE,化学药品仿制药口服固体制剂质量和疗效一致性评价申报资料要求,2016年第120号
[6] CDE,霍秀敏,ICH/WHO关于药物稳定性研究指导原则介绍,2003年11月08日
[7] CDE,张明平和霍秀敏,ICH确定新的稳定性试验条件的背景介绍,2004年04月20日
[8] CDE,黄晓龙,稳定性考察中的热循环(冻融)实验简介,2003年08月04日
[9] ICH(Q1B),稳定性试验: 新原料药和制剂的光稳定性试验,1996年11月06日
[10] ICH(Q1E),稳定性数据的评价,2003年02月06日
[11] ICH(Q1D),新原料药和制剂稳定性试验的括号设计法和矩阵设计法,2002年02月07日
[12] CDE,手性药物稳定性研究的几点认识,2005年09月14日
[13] CDE,霍秀敏,简略稳定性研究设计介绍,2005年05月13日
[14] 霍秀敏,魏农农,何伍,等.解读《化学药物(原料药和制剂)稳定性研究技术指导原则》[J].中国临床药理学杂志,2014(10):974-978.
撰稿人 | 药事纵横
责任编辑 | 胡静
审核人 | 何发
热点文章
-
一文搞定制药设备清洁验证分析方法的开发与验证
2024-03-12
-
偏差流程要点分析和偏差处理成熟度的考量
2024-02-29
-
工艺验证“连续三批”的含义?
2024-02-29
-
【汇总】药品GMP现场检查常见问题
2024-02-13
-
关于 B 证药品上市许可持有人供应商审计的思考
2024-03-01
-
中美医药数据出境监管新规对生物医药企业国际化影响及合规建议
2024-03-18
-
2024 AACR:中国双抗ADC们卷起来了?
2024-04-10
-
预约报名,免费参会|药品智能制造与质量控制技术交流会(5月16日,上海)
在新时代、新形势下,制药企业如何利用创新的生产模式和生产技术,持续打造数字化、低碳化的制药工程,实现生产过程高效灵活,推出满足国际药品质量标准的产品,是制药生产企业关注的重点。为了探讨和分析如何利用先进的技术、工艺和设备,快速、有效地进行药物产品开发、生产和质量管理,推动企业朝向高端化、绿色化和智能化发展。PharmaTEC制药业计划于5月16日(第90届中国医药原料药/中间体/包装/设备交易会期间),在上海举办“药品智能制造与质量控制技术交流会”,会议将以“数智赋能 质效双升”为主题,邀请制药行业专家,制药企业研发、生产、质量控制、工程和设施管理主管,从技术趋势、工艺优化、生产效率提升、成本节约、质量合规以及绿色智能节能等方面进行案例经验分享,以帮助制药企业应对绿色智能转型挑战,推动制药行业朝向高质量发展。
-
一种提高醇沉沉渣排放速度的方法
-
紫外光谱检测自制熊果酸片剂的含量
-
收藏 | 统计方法在药品工艺验证中的应用
-
火焰原子吸收光谱法测定左氧氟沙星氯化钠注射液中氯化钠的含量
-
新版附录1 对无菌灌装的影响










评论
加载更多