清洁验证中活性物质残留限度标准探讨
Part
1
1.1
目视检查
1.2
总有机碳(Total Organic Carbon,TOC) 标准
1.3
残留物浓度标准
1.4
基于药物活性数据的限度标准
1.5
基于药物毒理数据的限度标准
Part
2
2.1
各类限度标准的基本应用
2.2
残留限度标准应用的考虑
Part
3
3.1
残留限度标准制定不合理
3.2
具体标准限度数值制定依据不充分
3.3
清洁验证中未按验证方案规定项目进行全项检测
Part
4
参考文献
[1] 翟铁伟. 药品生产中清洁验证的生命周期探讨[J]. 中国医药工业杂志, 2019, 50(11) : 1341-1347.
撰稿人 | 叶笑、王立杰、颜若曦
责任编辑 | 胡静
审核人 | 何发
热点文章
-
一文搞定制药设备清洁验证分析方法的开发与验证
2024-03-12
-
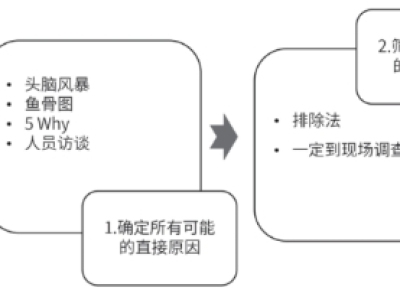
偏差流程要点分析和偏差处理成熟度的考量
2024-02-29
-
工艺验证“连续三批”的含义?
2024-02-29
-
【汇总】药品GMP现场检查常见问题
2024-02-13
-
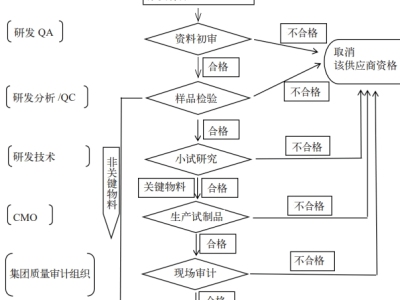
关于 B 证药品上市许可持有人供应商审计的思考
2024-03-01
-
中美医药数据出境监管新规对生物医药企业国际化影响及合规建议
2024-03-18
-
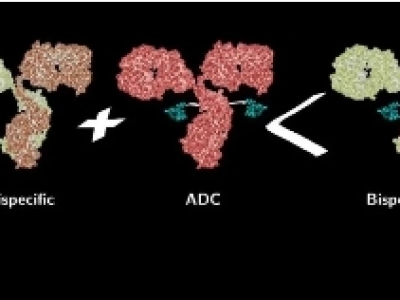
2024 AACR:中国双抗ADC们卷起来了?
2024-04-10
-
预约报名,免费参会|药品智能制造与质量控制技术交流会(5月16日,上海)
在新时代、新形势下,制药企业如何利用创新的生产模式和生产技术,持续打造数字化、低碳化的制药工程,实现生产过程高效灵活,推出满足国际药品质量标准的产品,是制药生产企业关注的重点。为了探讨和分析如何利用先进的技术、工艺和设备,快速、有效地进行药物产品开发、生产和质量管理,推动企业朝向高端化、绿色化和智能化发展。PharmaTEC制药业计划于5月16日(第90届中国医药原料药/中间体/包装/设备交易会期间),在上海举办“药品智能制造与质量控制技术交流会”,会议将以“数智赋能 质效双升”为主题,邀请制药行业专家,制药企业研发、生产、质量控制、工程和设施管理主管,从技术趋势、工艺优化、生产效率提升、成本节约、质量合规以及绿色智能节能等方面进行案例经验分享,以帮助制药企业应对绿色智能转型挑战,推动制药行业朝向高质量发展。
-
一种提高醇沉沉渣排放速度的方法
-
紫外光谱检测自制熊果酸片剂的含量
-
收藏 | 统计方法在药品工艺验证中的应用
-
火焰原子吸收光谱法测定左氧氟沙星氯化钠注射液中氯化钠的含量
-
新版附录1 对无菌灌装的影响










评论
加载更多